胰腺导管腺癌(PDAC)是一种高度侵袭性的癌症,生存机会很低。导致PDAC的分子触发因素仍不清楚。
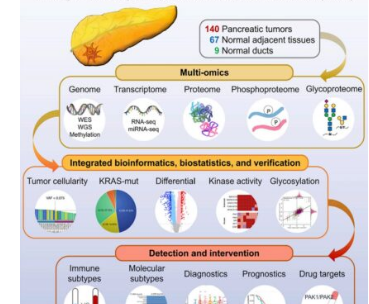
为了更好地了解PDAC背景下肿瘤发生的这些分子触发因素,由圣路易斯华盛顿大学、休斯顿贝勒医学院和巴尔的摩约翰霍普金斯大学的科学家领导的一个大型国际合作团队分析了蛋白质组和基因组研究人员对140例胰腺癌进行了研究,并将数据与67例正常周围组织和9例胰腺导管组织进行了比较。
除了分析蛋白质组如何通过磷酸化和糖基化进行修饰外,作者还对同一组织进行甲基化研究、全基因组和全外显子组测序以及RNA和microRNA测序,以全面了解基因组变化对细胞的影响。蛋白质表达、信号传导途径以及已合成蛋白质的生化修饰。作者采用多管齐下的方法,利用已确定的分子特征和组织学来分析肿瘤中的细胞变化。
这些发现发表在《细胞》杂志上的文章“胰腺导管腺癌的蛋白质组特征”中。这种全面、综合的蛋白质组学表征对于制定PDAC早期检测策略和识别治疗靶点来说是宝贵的资源。它通过对肿瘤基因和蛋白质的详细检查,确定了PDAC治疗和早期诊断的几个有前景的新靶点。
“这项研究中产生的大量数据可能有助于寻找新的方法来改善未来胰腺癌的检测和治疗,”合著者、索尔戈德曼胰腺癌研究中心主任、斯坦福大学教授、医学博士拉尔夫·赫鲁班(RalphHruban)说。约翰·霍普金斯大学医学院病理学。“这项研究是回答可能彻底改变胰腺癌治疗的研究问题的起点。”
“目前,胰腺癌患者的选择很少,而这项研究产生的大量数据可能会带来对抗这种疾病的新方法,”研究负责人、质谱核心设施主任、教授张辉博士说。约翰霍普金斯大学医学院病理学博士。
“尽管经过数十年的研究,胰腺癌的诊断结果仍然很严峻,”赫鲁班说。
诊断患有PDAC的患者五年生存率不到10%。对于疾病已扩散到身体其他部位(转移)的患者,中位生存期不到一年。由于缺乏早期诊断症状以及可靠的筛查和早期发现方法,大多数患者在无法进行手术时才确诊,导致预后不良。
张补充道:“尽管大量研究检查了胰腺肿瘤的基因,并发现了与这种疾病相关的几种突变,但这些突变不能通过药物治疗来靶向。”针对PDAC的免疫疗法并不是非常有效,因为这些肿瘤不会引起显着的免疫攻击。
为了找到更好的治疗靶点和标记物以早期检测胰腺癌,张赫鲁班、临床化学部主任兼病理学教授DanielChan博士、博士后研究员曹立伟博士以及来自约翰·霍普金斯大学等国际机构的合作者采用新的多组学方法,结合基因组学、转录组学和蛋白质组学。
研究人员证实,胰腺肿瘤更有可能在早期研究中报告的几个基因中发生突变,包括KRAS、TP53、CDKN2A和SMAD4。通过比较PDAC和正常细胞,研究小组发现了222种蛋白质,它们在癌细胞中的表达丰度是正常细胞的两倍。他们还确定了这222个蛋白质中近5,000个磷酸化增强的位点,以及超过1,700个糖基化增强(糖分子添加)的位点。
张说:“胰腺癌细胞会分泌几种糖基化蛋白质,”这表明它们有可能在血液中被检测到以进行早期诊断。
激酶通常代表细胞蛋白质组中的中心,通过向蛋白质添加磷酸基团来改变多种蛋白质的命运和功能。研究人员发现了PAK1和PAK2——两种在胰腺癌中失调的激酶,可以提供以前未被识别的治疗靶点。已知多种小分子抑制剂以PAK1为靶点,为治疗胰腺肿瘤提供了一条潜在途径。
张补充道:“癌细胞和正常组织之间的其他蛋白质差异似乎是阻碍免疫系统攻击的障碍。”他提出了可以针对这些蛋白质对PDAC肿瘤发起免疫攻击的新方法。
作者指出:“我们的研究描绘了驱动PDAC表型的分子特征,并为未来假设驱动的转化研究提供了丰富的生物信息资源。”

